| Fluoruro de Hidrógeno | ||
|---|---|---|
 | ||
 | ||
| General | ||
| Otros nombres | Ácido fluorhídrico (cuando está hidratado) | |
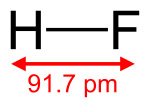
| Fórmula semidesarrollada | H-F | |
| Fórmula estructural | imagen superior | |
| Fórmula molecular | HF | |
| Identificadores | ||
| Número CAS | 7664-39-3[1] | |
| ChEBI | 29228 | |
| ChEMBL | CHEMBL1232767 | |
| ChemSpider | 14214 | |
| DrugBank | 11072 | |
| UNII | RGL5YE86CZ | |
| KEGG | C16487 | |
| Propiedades físicas | ||
| Apariencia | incoloro | |
| Densidad | 1140 kg/m³; 1,14 g/cm³ | |
| Masa molar | 20,0063 g/mol | |
| Punto de fusión | 190 K (−83 °C) | |
| Punto de ebullición | 293 K (20 °C) | |
| Propiedades químicas | ||
| Acidez | 3.17[2] pKa | |
| Solubilidad en agua | >70 g/100 ml agua (20 °C, 293 K) | |
| Momento dipolar | 1,98 D | |
| Peligrosidad | ||
| NFPA 704 |
0
4
2
COR
| |
| Riesgos | ||
| Riesgos principales | Muy alto | |
| LD50 | 180 mg/kg | |
| Más información | Cloruro de hidrógeno; Bromuro de hidrógeno; Fluoruro de sodio; Fluoruro de calcio; Teflón | |
| Valores en el SI y en condiciones estándar (25 ℃ y 1 atm), salvo que se indique lo contrario. | ||
El fluoruro de hidrógeno es un gas corrosivo. No se debe confundir con el ácido fluorhídrico, que es una disolución de fluoruro de hidrógeno (HF) en agua. No debe ponerse en contacto con elementos de vidrio ya que puede corroerlo, por esto se manipula bajo fríos extremos utilizando material de plástico.
YouTube Encyclopedic
-
1/3Views:1 5024143 460
-
Lewis Fluoruro de Hidrogeno
-
Union covalente de HF, fluoruro de hidrogeno o acido fluorhidrico V106
-
Selectividad PAU Química Madrid junio 2013 5A Equilibrio químico fluoruro de hidrógeno
Transcription
Datos fisicoquímicos
- LD50: 180 mg/kg.
- Concentración máxima permitida en los lugares de trabajo: 2 ppm.
Aplicaciones
El fluoruro de hidrógeno es un gas corrosivo que se utiliza en química orgánica en la obtención de compuestos orgánicos fluorados, como catalizador en petroquímica, para obtener criolita (Na3AlF6) artificial que se emplea en la obtención del aluminio, fluoruros inorgánicos como el hexafluoruro de uranio (UF6) y a veces como disolvente. También es utilizado en la industria y preparación de vidrio o cristal en el tallado y grabado del mismo. En estudios petrográficos de rocas graníticas es utilizado en estado puro para atacar con sus vapores los silicatos que componen la roca, para luego de un suave lavado con agua destilada ser cubierto con cobalto-nitrito de sodio el cual pintara selectivamente de un color amarillo intenso los feldespatos de potasio, que luego podrán ser distinguidos de los feldespatos plagioclasa sobre la base de su color y de esta manera se podrá clasificar la roca ígnea.
Toxicología
Se trata de una sustancia irritante, corrosiva y tóxica. En la piel produce quemaduras muy dolorosas de difícil curación. Esto se debe a que el calcio necesario en el proceso de curación precipita con los fluoruros como fluoruro de calcio (CaF2). En caso de haberse producido una quemadura con fluorhídrico se recomienda lavar con abundante agua "Kit de laboratorio", no agua corriente, y tratar como primera medida con un gel de gluconato de calcio (que debe estar disponible en todos los lugares donde haya o se maneje esta sustancia), en su defecto, utilizar una disolución de lactato cálcico o citrato cálcico o en su defecto con leche. En caso de aspiración de vapores, se trata de una emergencia médica. Se trata aplicando oxígeno por máscara (se desaconseja por irritantes otros materiales) si el afectado respira, controlando su nivel de conciencia. Llegado el caso, se debe aplicar resucitación de la persona afectada si fuera necesario. En caso de salpicaduras en los ojos, solamente tratar con solución fisiológica estéril en muy abundante cantidad; al igual que la respiración, se desaconseja por irritante sustancias basadas en compuestos cálcicos. En absolutamente todos los casos, se debe tratar en forma médica avanzada después de prestar los primeros auxilios.
Referencias
- ↑ Número CAS
- ↑ Harris, Daniel C. (2010). Quantitative Chemical Analysis (8th international edición). New York: W. H. Freeman. pp. AP14. ISBN 1429263091.
Enlaces externos
- ATSDR en Español - ToxFAQs: flúor, fluoruro de hidrógeno y fluoruros
- Hoja de datos de Seguridad (enlace roto disponible en Internet Archive; véase el historial, la primera versión y la última).

