La reacción de Passerini es una reacción química en la que se hacen reaccionar un isocianuro , un aldehído (o cetona ), y un ácido carboxílico para formar una α- aciloxiamida.[1][2][3]
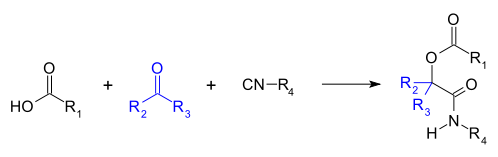
Esta reacción orgánica fue descubierta por Mario Passerini en 1921 en Florencia , Italia . Es la primera reacción multicomponente basada en isocianuro desarrolladas, y en la actualidad juega un papel central en la química combinatoria.[4]
Recientemente, Denmark y colaboradores han desarrollado un catalizador enantioselectivo para reacciones asimétricas de Passerini.[5]
YouTube Encyclopedic
-
1/1Views:2 745
-
The Ugi Reaction: Reaction mechanism chemistry tutorial.
Transcription
Mecanismo de Reacción
Se han propuesto dos mecanismos de reacción diferentes:
Mecanismo iónico
En disolventes polares como metanol o agua , se lleva a cabo la reacción de protonación del carbonilo (1) seguida por la adición nucleofílica del isocianuro (2) para dar el ion nitrilio de la cianhidrina formada (3) . A su vez, una molécula de carboxilato se adiciona al carbono del ion formado para producir un anhídrido mixto carboxílico-carboximídico (4) .El grupo acilo del anhídrido transpone hacia el hidroxilo cianhidrínico y el carboximidato tautomeriza a amida para producir el éster deseado (5)
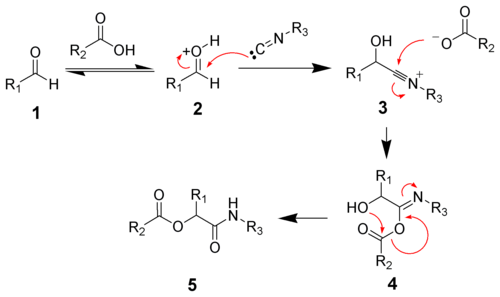
Mecanismo concertado
En solventes no polares, y a una alta concentración, es probable un mecanismo concertado:[6]

:
Este mecanismo consiste en una reacción trimolecular entre el isocianuro (R-NC), el ácido carboxílico, y el carbonilo en una secuencia de adiciones nucleofílicas . El estado de transición TS #se representa como un anillo de 5 miembros con uniones covalentes parciales o dobles. El segundo paso de la reacción de Passerini es una transferencia de acilo al grupo hidroxilo vecinos. El sustento teórico de este mecanismo de reacción es que la reacción procede en disolventes relativamente no polares (en línea con el estado de transición) y la cinética de la reacción depende de los tres reactivos . Esta reacción es un buen ejemplo de una síntesis convergente .
Aplicaciones
Las reacción de Passerini se utiliza en muchas reacciones de componentes múltiples , por ejemplo, una de ellas va precedida por una reacción de Horner-Wadsworth-Emmons y el producto formado es un depsipéptido:[7]

Se han explorado aplicaciones de las reacciones Passerini para su uso en la preparación de polímeros a partir de materiales renovables.[8]
Véase también
Referencias
- ↑ Passerini, M.; Simone, L. Gazz. Chim. Ital. 1921, 51, 126-129.
- ↑ Passerini, M.; Ragni, G. Gazz. Chim. Ital. 1931, 61, 964-969.
- ↑ Banfi, L.; Riva, R. (2005). «The Passerini Reaction». Org. React. 65: 1-140. doi:10.1002/0471264180.or065.01..
- ↑ Dömling, A.; Ugi, I. Angew. Chem. Int. Ed. Engl. 2000, 39, 3168-3210. (Review)
- ↑ Denmark, S. E.; Fan, Y. J. Org. Chem. 2005, 70, 9667-9676.doi 10.1021/jo050549m
- ↑ The Passirini Reaction L. Banfi, R.Riva in Organic Reactions vol. 65 L.E. Overman Ed. Wiley 2005 ISBN 0-471-68260-8
- ↑ A Flexible Six-Component Reaction To Access Constrained Depsipeptides Based on a Dihydropyridinone Core Monica Paravidino, Rachel Scheffelaar, Rob F. Schmitz, Frans J. J. de Kanter, Marinus B. Groen, Eelco Ruijter, and Romano V. A. Orru J. Org. Chem. 2007, 72, 10239-10242 doi 10.1021/jo701978v
- ↑ Kreye, O.; Tóth, T.; Meier, M. J. Am. Chem. Soc., 2011, 133 (6), pp 1790–1792 DOI: 10.1021/ja1113003
